ATOMÍSTICA - HISTÓRICO DO ÁTOMO - PARTE 1
A)
MILETO E DEMÓCRITO ® 400 a.C., os
filósofos gregos elaboraram a filosofia do átomo. À menor porção da matéria,
eles deram o nome de átomo (que em grego significa indivisível e
indestrutível). Para eles, a natureza era formada por átomos e vácuo.
B - JOHN DALTON ® Cientista criador do 1º modelo
atômico. Para ele o átomo era uma pequena bolinha maciça e indivisível. Ainda
segundo Dalton, o número de átomos diferentes na natureza era pequeno, e a
formação da matéria se dava através de átomos iguais ou átomos diferentes (átomos
compostos).
A matéria era
formada por átomos junta postos, isto é, uns colados aos outros, não havendo
espaços vazios entre eles.
Dalton também foi
responsável pela criação da Lei das Proporções Múltiplas. Foi um membro
destacado da comunidade Quaker (lembrar da embalagem da Aveia Quaker), tendo
sido o primeiro cientista a descrever uma deficiência visual da qual o mesmo
sofria (daltonismo).
Assim seria o
modelo do átomo imaginado por Dalton:
Para Dalton as substâncias se dividiam em
compostas (átomos compostos), quando eram formadas por átomos diferentes aos
pares ou em três, e simples (átomos simples), quando eram formadas por átomos
iguais aos pares ou em três.
EVOLUÇÃO DA TEORIA ATÔMICA
Surgem as Leis de
Lavoisier: Numa reação química a soma das massas dos reagentes é igual à dos
produtos (Lei da Conservação da Matéria),
de Proust: Numa reação química as massas das substâncias participantes guardam
entre si uma mesma proporção (Proporções
Constantes) e de Dalton: Quando uma massa fixa de um elemento A reage com
massas diferentes de outro elemento B, dando compostos diferentes, as massas de
B guardam entre si uma relação expressa por números inteiros e pequenos. (Proporções Múltiplas).
Franklin observou
duas espécies de partículas elétricas, arbitrariamente denominadas de positiva e negativa. Também observou que cargas de sinais opostos se atraem e
de mesmo sinal se repelem.
GEISSLER E PLUCKER - Fazem passar uma corrente elétrica
através de um tubo contendo gás rarefeito, (submetido à baixa pressão ou
pressão reduzida) e observam o surgimento de uma luz esverdeada, todavia não
chegam a uma conclusão final sobre a origem da luz.
EUGEN GOLDSTEIN ® Ao
estudar os raios catódicos em uma ampola de Crookes,
Eugen Goldstein introduziu em 1886 uma nova variante na experiência: perfurou o cátodo da ampola e percebeu um feixe
de raios de luz (os quais deu o nome de raios canais) na direção oposta ao
feixe dos raios catódicos. Se os raios catódicos eram negativos, este novo raio
deveria ter um caráter positivo. No entanto, Goldstein não compreendeu exatamente o que acontecia e o
assunto foi esquecido por alguns anos.
EXPERIÊNCIAS DE GOLDSTEIN
1.ª EXPERIÊNCIA
→ Sem alterar a pressão.
→ Colocou gás (ar) no interior
do tubo e observou que não ocorreu descarga elétrica, a não ser em voltagens
elevadíssimas (o que ocorre nas tempestades).
2.ª EXPERIÊNCIA
Reduziu a pressão (condição para condução
da corrente elétrica no ar e em outros gases).
Notou o aparecimento de fluorescência
esverdeada no tubo mais próximo da parede oposta do cátodo.
Isso ocorre devido a ionização das
moléculas dos gases. Esses raios recebem o nome de raios catódicos.
EXPERIÊNCIA DE WILLIAN CROOKES
Constrói
um aparelho para melhor estudar esses raios, é a AMPOLA DE CROOKES.
→ Coloca o cátodo
(-) ao lado do ânodo.
EXPERIÊNCIAS E CONCLUSÕES
1ª) A mudança do ânodo não altera a trajetória dos raios
catódicos.

|
→ Note que o cátodo
não é curvilíneo.
→ Note que o cátodo
é curvilíneo.
PROPRIEDADE
– Observou que os raios catódicos são perpendiculares ao cátodo.
2ª) Colocando um
anteparo no interior da ampola observou a formação de uma sombra na parede
oposta ao cátodo.
PROPRIEDADE
– Observou que os raios catódicos são retilíneos.
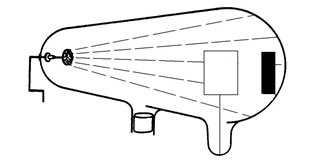
3ª) Colocando-se um objeto com eixo livre, no caso, a
estrela, na trajetória do raio, a mesma passou a girar, evidenciando que algo
sólido colide com ela.
PROPRIEDADE
– Observou que os raios catódicos têm massa.
4ª)
Submete os raios catódicos a um campo elétrico, para provar que sofrem desvios
na direção da placa positiva.
PROPRIEDADE
– Observou que os raios catódicos têm carga negativa. Denominou-se de elétrons.
Os prótons são os raios anódicos.
ACONTECIMENTOS QUE CONTRIBUÍRAM PARA A
EVOLUÇÃO DOS NOVOS MODELOS ATÔMICOS
A DESCOBERTA DA RADIOATIVIDADE - Roentgen
descobre acidentalmente os raios X, possibilitando Becquerel descobrir a
radioatividade e o primeiro elemento capaz de emitir radiação (urânio).
Note que, com estas
descobertas podemos fazer dois questionamentos. Se o átomo é indivisível e por consequência
a matéria também, como algo podia atravessa-la (Raio X) ou sair dela? (Radiação).
Isto leva os cientistas a desconfiar da divisibilidade do átomo.
A seguir Ernest Rutherford descobre os raios
alfa e beta, que após estudados tinham propriedades:
Raios α - partículas pesadas e positivamente
carregadas, pouco penetrantes;
Raios β - partículas leves e negativamente
carregadas mais penetrantes que os raios;
Realiza
experimentos com a ampola de Goldstein e detecta presença de partículas
positivas ainda menores, as quais batizou prótons, e segundo seus cálculos, é
cerca de 1.836 vezes maior do que o elétron.
PAUL VILLARD – descobre as radiações eletromagnéticas,
mais penetrantes e sem carga elétrica, semelhante aos raios X, denominando-as
de raios gama (γ).
C) MODELO DE J. J.
THOMSON ® Trabalhando em tubos de pressão reduzida,
verificou que nos átomos existem cargas negativas, inicialmente batizadas de
raios catódicos, e só posteriormente batizadas de etrons (partículas
subatômicas assim como os prótons) por Stoney.
Cria o modelo atômico conhecido como “pudim de passas”.
Para ele, o átomo seria uma esfera positiva incrustada de elétrons.
As esferas escuras
são os elétrons e o restante dos átomos seria formado por um fluído com carga
positiva.
Thomson,
com o seu modelo, procura explicar fenômenos que o de Danton não explicava,
tais como: eletricidade, radicação, raios x, ... Nele, destacou o átomo como
estrutura elétrica (estrutura neutra, onde as partículas positivas
neutralizariam as partículas negativas).
Thomson
já sabia da divisibilidade do átomo, só não teve como comprova-lo, que é o que
veremos agora.
PELO PROFESSOR EUDO ROBSON
ESTA AULA ESTÁ DISPONÍVEL PARA DOWNLOAD GRATUITO NO SITE: www.universodaquimica.com
FIM DA PARTE 1




















Sem comentários:
Enviar um comentário